問4
雲の中の降水粒子の成長について述べた次の文 (a) ~ (d) の正誤の組み合わせとして正しいものを、下記の1~5の中から1つ選べ。
(a) 雲内での水滴の併合過程では、単位体積に含まれる水滴の質量の合計が同じであれば、大きさの異なる水滴が多数存在している場合よりも、大きさが一様な水滴が多数存在している場合の方が、水滴が速く成長する。
(b) 過冷却水滴を含む雲内に生成された氷晶は、過冷却水滴と衝突・併合する過程がないと雪に成長して地上に降ってくることはできない。
(c) 凝結核を持たずに形成された純水の微小水滴では、表面張力の作用により、水滴が小さいほど、より小さな過飽和度で水蒸気が凝結する。
(d) 水溶性のエーロゾルを凝結核として形成された微小水滴は、同じ大きさの純水の微小水滴よりも、水滴の表面に対して平衡する水蒸気圧が低いため、凝結による成長が起こりやすい。
水滴の終端速度(予備知識)

水滴が重力によって落下し始めると、落下速度は重力加速度に従って大きくなります。
そして、ある速さに達すると重力と空気抵抗が釣り合い、水滴の落下速度は一定になります。
この一定になった速度を水滴の終端速度といいます。
水滴の終端速度 \( V \) は、以下のように重力 \( mg \) と空気抵抗 \( 6 \pi r \eta V \) の釣り合いから求めることができます。
\( mg = 6 \pi r \eta V \)
水滴の質量 \( m = \displaystyle \frac{4}{3}\pi r^3 \rho \) を代入して式変形すると
\( V = \displaystyle \frac{2 \rho r^2 g}{9 \eta} \)
となり、水滴の終端速度 \( V \) は水滴の半径の2乗 \( r^2 \) に比例します。
( \( V \):水滴の終端速度、\( \rho \):水の密度、\( r \):水滴の半径、\( g \):重力加速度、\( \eta \):流体の粘性係数(粘度ともいう))
飽和水蒸気圧(予備知識)
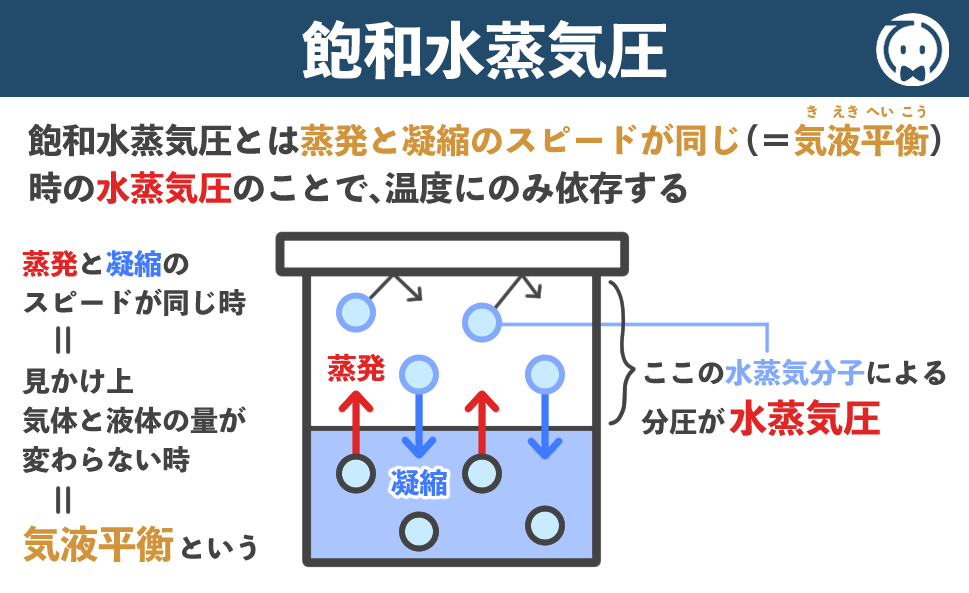
密閉した容器内で蒸発(水→水蒸気)と凝縮(水蒸気→水)のスピードが同じになり、見かけ上、気体(水蒸気)と液体(水)の量が変わらない状態を気液平衡(読:きえきへいこう)といいます。
そして、気液平衡の時の水蒸気分子による分圧を飽和水蒸気圧(読:ほうわすいじょうきあつ)といい、飽和水蒸気圧は温度にのみ依存します。
例えば、密閉容器に少量の液体を入れて温度を一定にすると、
最初のうちは蒸発する分子の数は一定ですが、時間が経つと凝縮する分子の数が増加していきます。
しばらくすると、一定時間あたりに蒸発する分子と凝縮する分子の数が等しくなり、見かけ上は蒸発も凝縮も起こっていない状態になります。
このときの状態を気液平衡といい、気液平衡時の水蒸気分子による分圧を飽和水蒸気圧といいます。
また、飽和水蒸気圧は温度が上がるにつれて大きくなります。
温度が高いほど、蒸発が進むので水蒸気量が多くなるため、飽和水蒸気圧も大きくなります。
一方、飽和水蒸気圧は気体の体積には関係なく一定です。
体積を増加させるとその分蒸発が進み、体積を減少させると凝縮が進み、やがて平衡状態に達するため、飽和水蒸気圧は一定となるのです。
これは他の気体が共存していても変わりません。
水面と氷面の飽和水蒸気圧(予備知識)
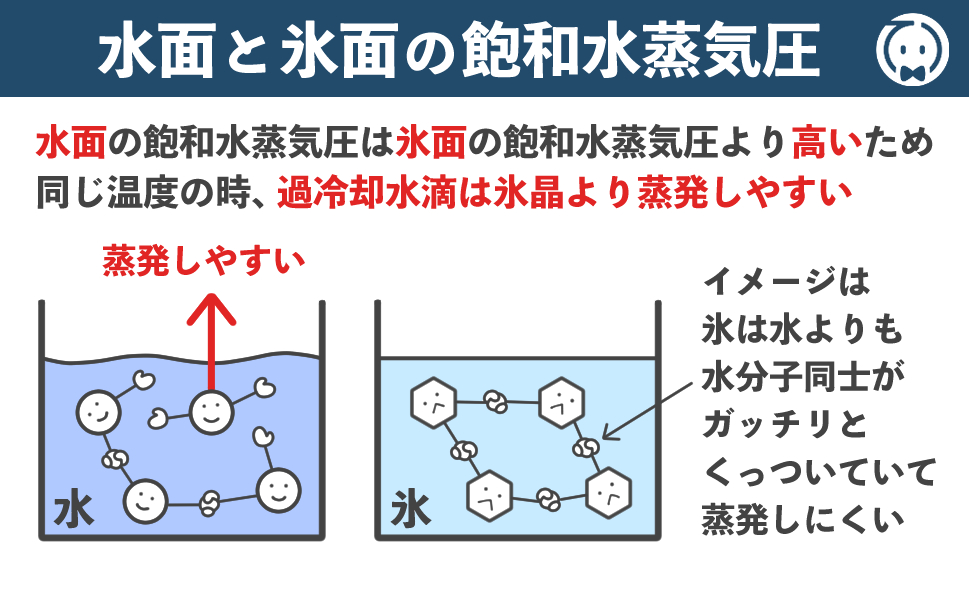
同じ温度の時、水面に対する飽和水蒸気圧は氷面に対する飽和水蒸気圧より高くなります。
 てるるん
てるるんイメージとしては、氷の結晶はガッチリと手を繋いでくっついているので蒸発しにくいけど、水は氷よりも手を繋ぐ力が弱いので蒸発しやすい、という感じだね!
こうして水滴から蒸発してできた水蒸気は氷晶に向かって拡散していき、氷晶にくっついて(=昇華して)氷晶が成長します。
本問の解説:(a) について
(問題)雲内での水滴の併合過程では、単位体積に含まれる水滴の質量の合計が同じであれば、大きさの異なる水滴が多数存在している場合よりも、大きさが一様な水滴が多数存在している場合の方が、水滴が速く成長する。
→ 答えは 誤 です。
水滴の終端速度は以下の式で表すことができます。
\( \displaystyle V = \frac{2 \rho r^2 g}{9 \eta} \propto r^2 \)
( \( V \):水滴の終端速度、\( \rho \):水の密度、\( r \):水滴の半径、\( g \):重力加速度、\( \eta \):流体の粘性係数(粘度ともいう))
終端速度とは、水滴にかかる重力と空気抵抗が釣り合って、一定になった落下速度のことです。



簡単に言うと、この式は水滴の終端速度 \( V \) が水滴の半径の2乗 \( r^2 \) に比例する、ということを表しているよ!
つまり、水滴の終端速度 \( V \) は水滴の半径 \( r \) によって決まり、水滴の半径 \( r \) が大きいほど水滴の終端速度 \( V \) は大きくなります。
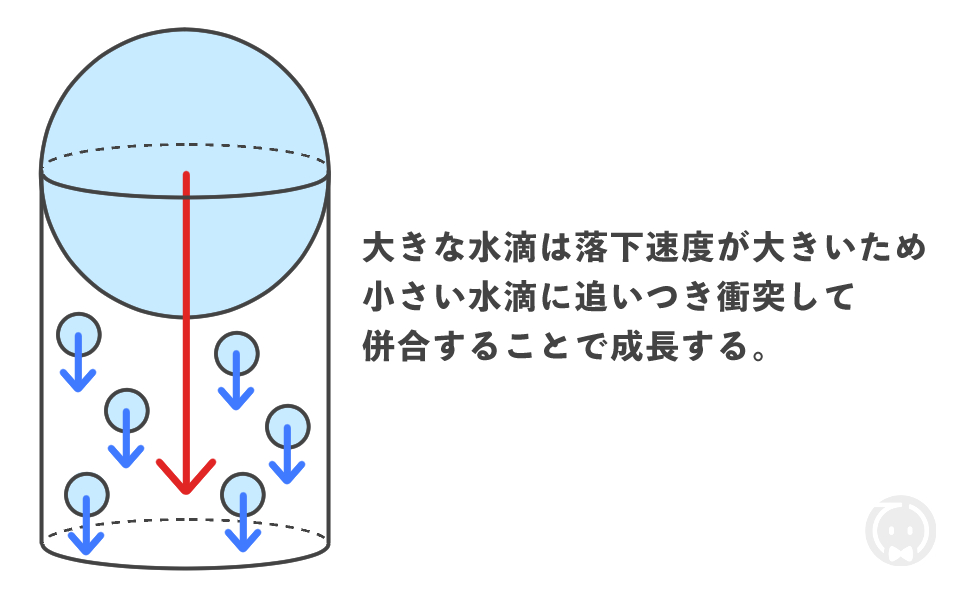
また、水滴の併合過程では、大きさと落下速度の違う水滴たちが衝突することで水滴が成長します。
大きな水滴は落下速度が大きいため、小さい水滴に追い付き、衝突して併合することで成長します。
もし、すべての水滴の大きさが同じだったら、すべての水滴の落下速度は等しくなり、水滴同士があまりぶつからないため、成長のスピードは遅くなります。

もちろん、これは単位体積に含まれる水滴の質量の合計が同じであるという条件のもとです。



水滴の大きさが異なっていても、空気中に水滴が全然なければ、そもそもぶつからないからね!
したがって、単位体積に含まれる水滴の質量の合計が同じであれば、大きさが一様な水滴が多数存在している場合よりも、大きさの異なる水滴が多数存在している場合の方が、水滴が速く成長するので、答えは 誤 となります。
本問の解説:(b) について
(問題)過冷却水滴を含む雲内に生成された氷晶は、過冷却水滴と衝突・併合する過程がないと雪に成長して地上に降ってくることはできない。
→ 答えは 誤 です。
氷晶の成長過程は3種類あります。
(1)水蒸気の昇華凝結による成長
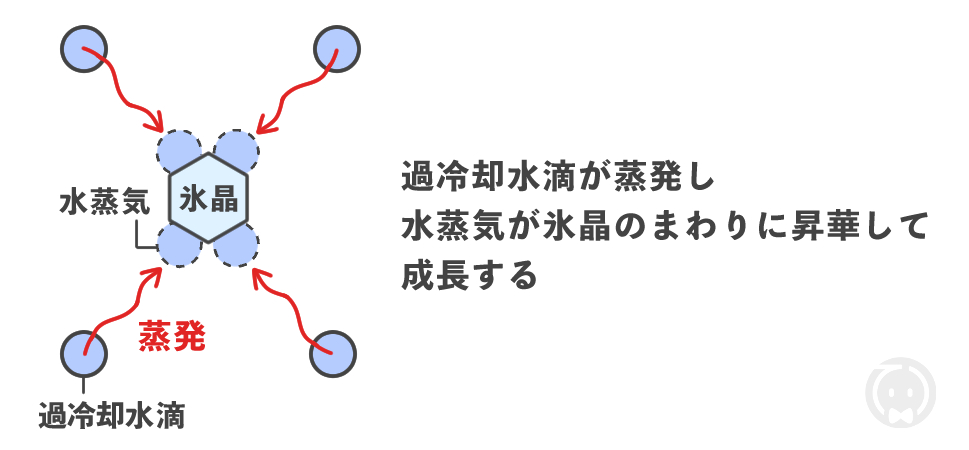

過冷却水滴が蒸発し、水蒸気が氷晶のまわりに昇華することで氷晶が成長します。
水蒸気が昇華凝結して氷晶が成長する過程には、水と氷の飽和水蒸気圧の差が関係しています。
実は氷点下において、水面に対する飽和水蒸気圧は氷面に対する飽和水蒸気圧より高くなっています。
言い換えると、同じ温度であれば、過冷却水滴に対して飽和している時、氷に対してはすでに過飽和の状態であるということです。
例えば、-20℃の雲の中では、氷晶に対してちょうど飽和していても、過冷却水滴に対しては未飽和なので、過冷却水滴はまだまだ蒸発します。
こうして蒸発してできた水蒸気がどんどん氷晶の方に昇華していき、氷晶が成長します。
(2)過冷却水滴との衝突による成長
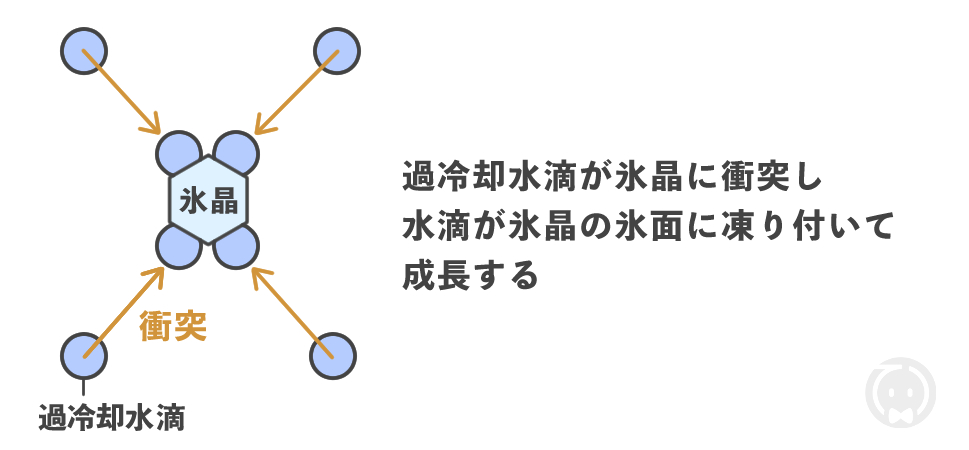

過冷却水滴が氷晶に衝突し、水滴が氷晶の氷面に凍り付くことで氷晶が成長します。
この過程をライミング(riming)と呼びます。
特に、発達した雲の中で強い上昇流・下降流がある時は、成長した氷晶が繰り返し上下運動をすることで、さらに大きくなり「あられ」や「ひょう」になることもあります。
(3)氷晶同士の衝突による成長
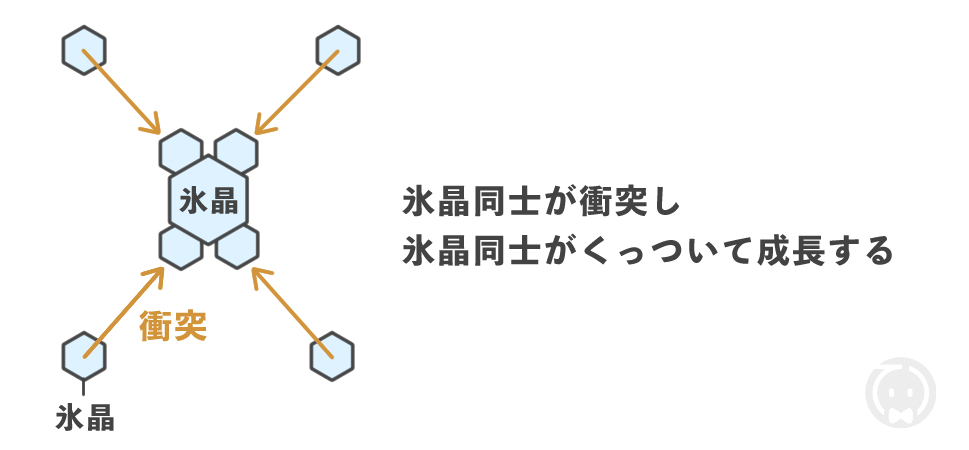

氷晶同士が衝突し、氷晶同士がくっ付くことで氷晶が成長します。
この過程を凝集(aggregation)と呼びます。
氷晶の落下速度は形や大きさによって異なります。
このため、落下速度が異なる氷晶同士がぶつかって、合体することで氷晶が成長します。
ここで、本問題を考えてみましょう。
「過冷却水滴を含む雲内に生成された氷晶は、過冷却水滴と衝突・併合する過程がないと雪に成長して地上に降ってくることはできない」というのは正か誤か、という問題です。
この問題を言い換えると「(2)過冷却水滴との衝突による成長」がないと雪に成長して地上に降ってこない、というのは正か誤か、となります。
したがって、氷晶の成長過程は「(2)過冷却水滴との衝突による成長」の他に「(1)水蒸気の昇華凝結による成長」と「(3)氷晶同士の衝突による成長」があるため、答えは 誤 となります。
本問の解説:(c) について
(問題)凝結核を持たずに形成された純水の微小水滴では、表面張力の作用により、水滴が小さいほど、より小さな過飽和度で水蒸気が凝結する。
→ 答えは 誤 です。
空気中の水蒸気が増え、相対湿度が100%に達すると、水蒸気が凝結して水滴となります。
しかし、相対湿度が100%を超えても、水蒸気がまだ存在していることがあります。
この状態を過飽和(読:かほうわ)と呼びます。



過飽和状態では、湿度が100%を超えているわけだけど、どれくらい超えているかを表すのが過飽和度だよ!
過飽和度は、相対湿度から100%を引いた値です。
過飽和度(%) = 相対湿度(%) - 100%
例えば、相対湿度が110%の場合、過飽和度は10%となります。
過飽和が起こる原因は 表面張力 です。
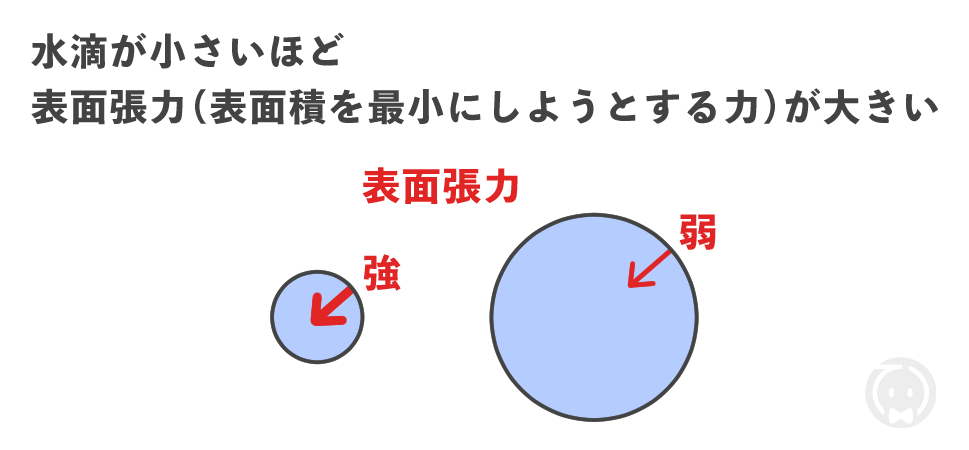
表面張力は水滴にはたらく力で、水滴の表面積を最小にしようとする力です。
水滴が⼩さいほど、表面張力は強くなります。

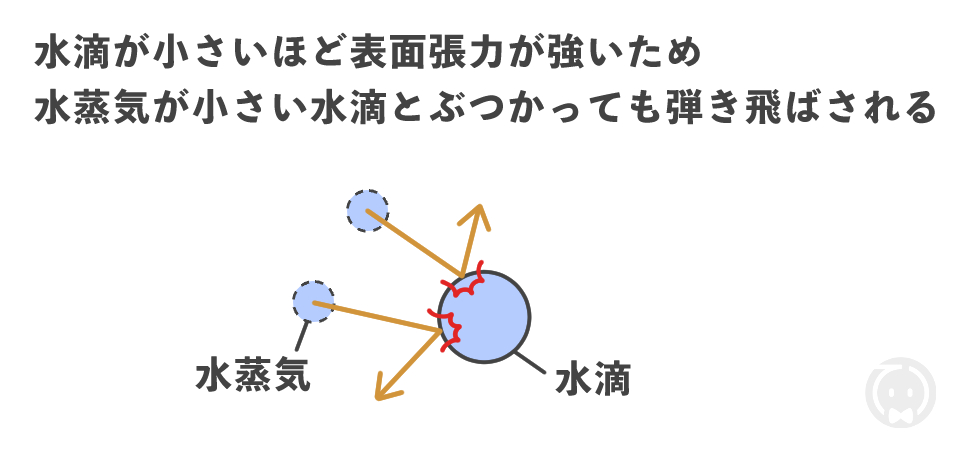
水蒸気が水滴に凝結するためには、水蒸気の分子が水滴に衝突して結合する必要があります。
しかし、水滴の半径が小さいほど表面張力(=表面積を大きくしないようにする力)が強いため、水蒸気が小さい水滴とぶつかっても、結合せずに弾き飛ばされてしまいます。
その結果、水滴になれない水蒸気が多く存在するようになり、過飽和度は高くなります。

過飽和度が高くなると、空気中の水蒸気量が増えるので水蒸気圧は飽和水蒸気圧よりも高くなります。
そうして、高い圧力で小さい水滴にぶつかるようになって初めて水滴が成長します。
下図は水滴の半径と過飽和度の関係を表したグラフです。
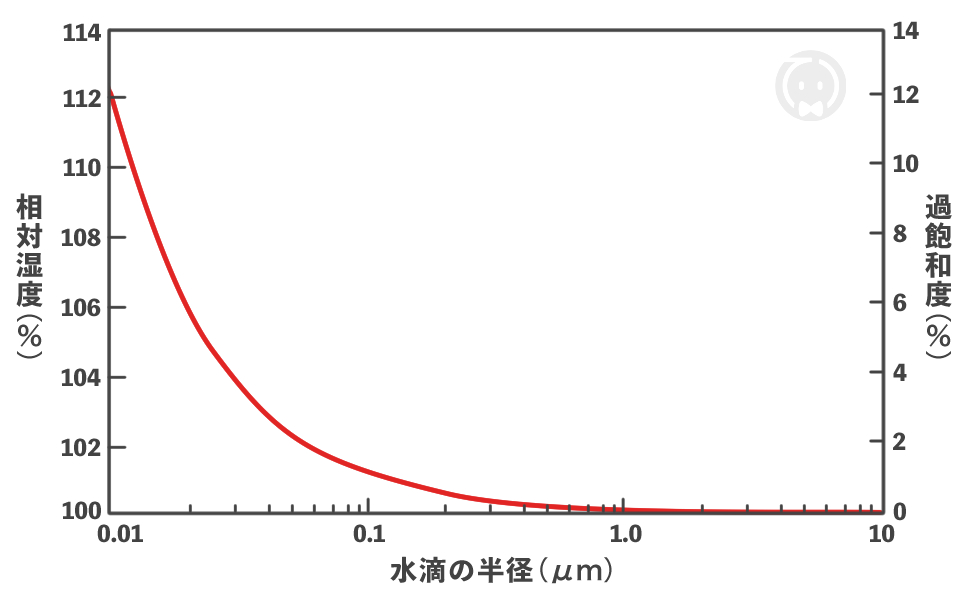

このグラフは水滴が成長するのに必要な過飽和度を表している、と考えることができます。



例えば、半径 1 μm の水滴が成長するためには、過飽和度が 0.1 % あれば十分だけど、半径 0.01 μm の水滴が成長するためには、過飽和度が 12 % に達しないと成長できないよ!
つまり、水滴の半径が小さいほど、成長するためには大きな過飽和度が必要ということです。
(しかし、実際には自然界で過飽和度が1%を超えることはまれなので、このような水滴は成長できずにすぐに蒸発してしまいます。)
したがって、凝結核を持たずに形成された純水の微小水滴では、水滴が小さいほど水蒸気が凝結するためにはより「小さな」過飽和度ではなく「大きな」過飽和度が必要であるため、答えは 誤 となります。
本問の解説:(d) について
(問題)水溶性のエーロゾルを凝結核として形成された微小水滴は、同じ大きさの純水の微小水滴よりも、水滴の表面に対して平衡する水蒸気圧が低いため、凝結による成長が起こりやすい。
→ 答えは 正 です。
一般に化学物質が溶けた水(=溶液)に対する飽和水蒸気圧は、純粋な水の飽和水蒸気圧より低いという性質があります。



例えば、水によく溶ける食塩(NaCl)で考えてみよう!
温度が 18 度のとき、純粋な(平面の)水面に対する飽和水蒸気圧は 20.6 hPa です。
しかし、1 kg の水に 100 g の食塩が溶けた溶液に対する飽和水蒸気圧は 19.6 hPa であり、
限界の 357 g が溶けた溶液ではわずか 15.6 hPa で、純水な水の約 76 % しかありません。
したがって、相対湿度が 約 76 % 以上あれば、食塩は水蒸気を吸収して溶けることができます。
(※ただし、これは平面の溶液に対する飽和水蒸気圧であり、エーロゾルが溶けて液滴となったときの飽和水蒸気圧を考えるには、液滴の曲率も考慮しなければなりません。)
つまり何が言いたいのかというと、水溶性のエーロゾルは相対湿度が低くても水に溶けやすく、それによって形成された微小水滴(=溶液)は、同じ大きさの純水の微小水滴よりも、水滴の表面に対して飽和水蒸気圧が低くなる、ということです。
飽和水蒸気圧が低いということは、より多くの水蒸気が凝結して成長しやすいということです。
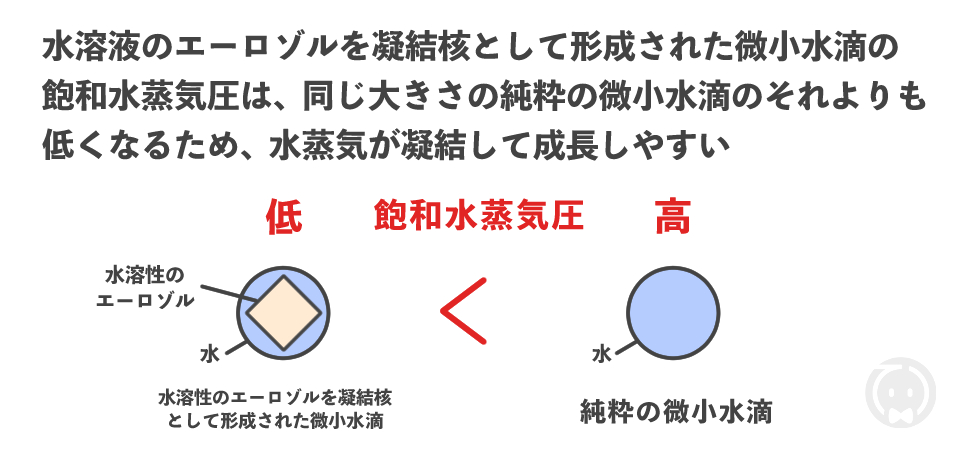

したがって、水溶性のエーロゾルを凝結核として形成された微小水滴は、同じ大きさの純水の微小水滴よりも、水滴の表面に対して平衡する水蒸気圧が低く、凝結による成長が起こりやすいため、答えは 正 となります。
以上より、本問の解答は (a) 誤 (b) 誤 (c) 誤 (d) 正 とする 5 となります。
書いてある場所:P78〜81(表面張力、過飽和度)、P81〜85(エーロゾル、凝結核)、P89〜90(水滴の併合過程)、P94〜98(氷粒子の成長)
書いてある場所:P65〜67(表面張力、混合比)、P67〜68(エーロゾル、凝結核)、P69(水滴の併合過程)、P69〜70(氷粒子の成長)、P71〜72(雲粒の終端速度)
試験問題は「一般財団法人 気象業務支援センター」様の許可を得て掲載しています。
当記事の解説は「一般財団法人 気象業務支援センター」様とは無関係ですので、情報の誤りや不適切な表現があった場合には、お問い合わせからご連絡ください。
また、当記事に掲載された内容によって生じた損害等の一切の責任を負いかねますのでご了承ください。



コメント
コメント一覧 (2件)
「凝縮」という単語が多用されていますが、「凝結」ではないでしょうか?
ヒビカセ様
コメントありがとうございます。
「凝縮」と「凝結」はどちらも、気体が液体に変化することを意味します。
これらの使い分け方に明確な基準はありませんが、一般に「凝縮」は、物理・化学の分野で使われることが多く、「凝結」は、気象学において使われることが多いです。
本記事で使用している「凝縮」という言葉は、「気液平衡」を説明するために使用しています。
「気液平衡」は、一般に化学の分野で使われる言葉ですので、本記事でも「気液平衡」を説明する時のみ「凝縮」を使用しています。
(実際に「気液平衡」についてgoogleで調べてみると、「凝結」ではなく「凝縮」が使われていることが多いです。)
それ以外の、氷晶の成長過程など、気象学に関する部分については「凝結」を使用しています。
よろしくお願いいたします。